Brustkrebs im Frühstadium
Mit über 70.000 Neuerkrankungen pro Jahr ist der Brustkrebs ein häufig vorkommender Tumor. Das Risiko einer Erkrankung steigt mit dem Alter an und die Diagnose löst oft Ängste und Sorgen aus. Entsprechende Früherkennungsprogramme und moderne Diagnosemethoden ermöglichen immer häufiger eine frühzeitige Erkennung. Im Frühstadium diagnostiziert kann Brustkrebs oft geheilt werden. Durch unterschiedlichste Tumormarker (Biomarker) können neue Therapiemöglichkeiten zum Einsatz kommen oder es werden spezifisch gegen diese Marker Therapien entwickelt. Zu diesen Markern gehören vor allem der sogenannte „Humane Epidermale Wachstumsfaktorrezeptor 2“ (kurz „HER2-Rezeptor“), der Hormonrezeptor (kurz „HR“) und der Tumormarker Ki-67.
Tripel-positive Patienten
Haben Sie im Zusammenhang mit Brustkrebs schon den Begriff „tripel-positiv“ gehört? Oder auch co-positiv?
Diese Begriffe bezeichnen Tumore, die sowohl HER2+ als auch HR+ sind.
Für die Behandlung dieser Tumore stehen zielgerichtete Therapien zur Verfügung,
über die wir Ihnen einen kurzen Überblick geben wollen.
HER2-Rezeptorstatus
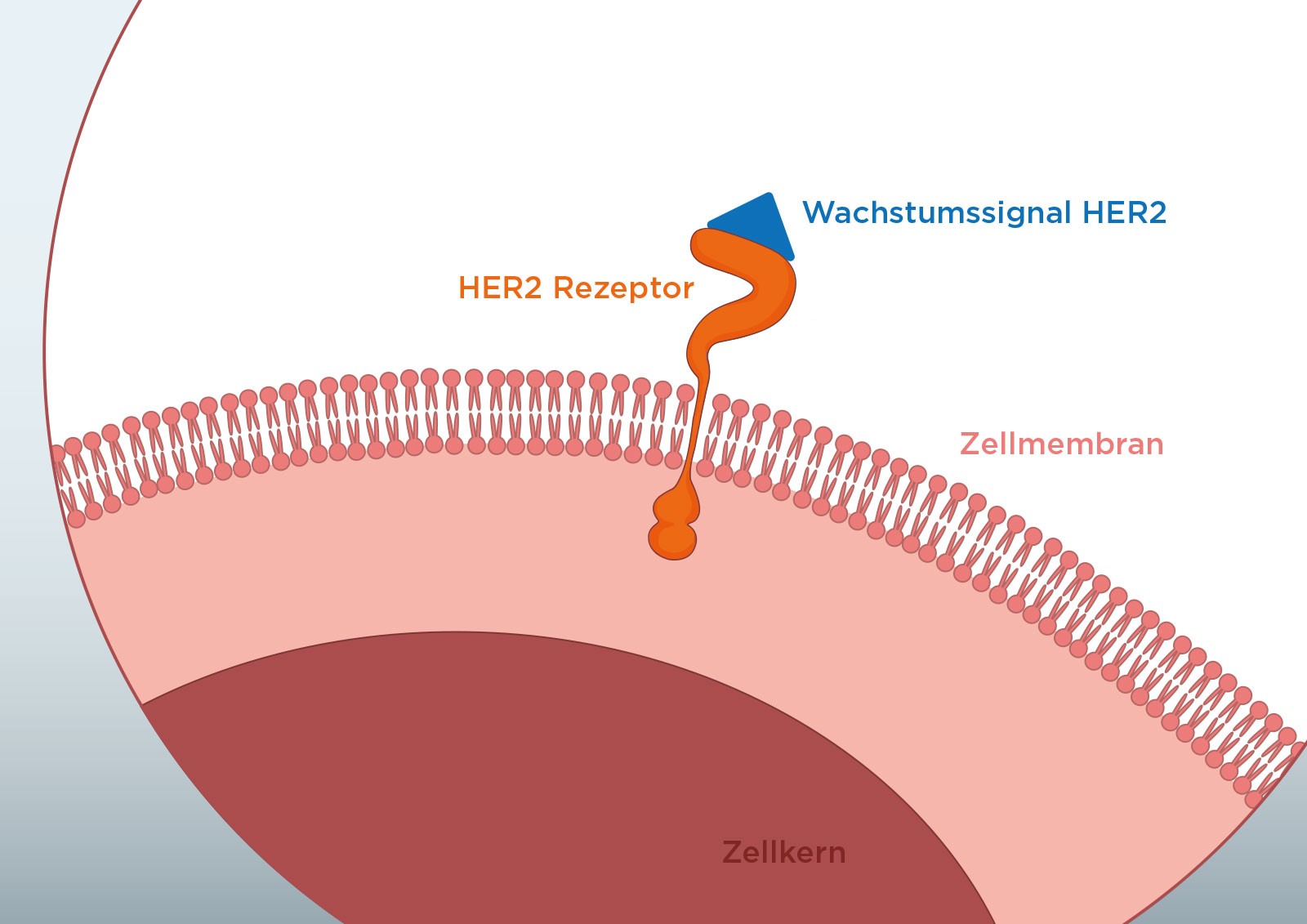
Der HER2-Rezeptor ist ein Protein, dass für ein gesundes Wachstum von Zellen notwendig ist. Sind die Zellen gesund, besitzen sie nur eine geringe Menge dieses Rezeptors auf ihrer Zelloberfläche. Ist die Anzahl der HER2-Rezeptoren stark erhöht, führt dies zu einer höheren Teilungsrate – diese Zellen nennt man HER2-positiv bzw. HER2+. Mit zielgerichteten Therapien lassen sich HER2-Rezeptoren blockieren und das Tumorwachstum einschränken.
Hormonrezeptorstatus (HR)
Der Hormonrezeptor (HR)-Status gibt Auskunft darüber, ob der Tumor auf Hormone wie Östrogen und Progesteron anspricht. In diesen Fällen fördern Hormone das Tumorwachstum – man bezeichnet den Tumor als hormonabhängig. Etwa zwei Drittel aller Brustkrebsarten haben einen positiven HR-Status (kurz HR+). Der Einsatz einer antihormonellen Therapie kann das Wachstum solcher Tumore verlangsamen oder stoppen.
Warum zielgerichtete Therapien
Vielleicht haben Sie schon von zielgerichteten Therapien oder auch dem englischen Begriff „targeted therapies“ gehört. Grundsätzlich gibt es verschiedene Möglichkeiten Krebs zu bekämpfen. Wenn Medikamente verabreicht werden, sollen diese möglichst gegen die Krebszellen wirken, ohne gesunde Zellen zu schädigen. Krebszellen sollen am Wachstum gehindert und idealerweise soll der Zelltod herbeigeführt werden. Dafür gibt es unterschiedliche Strategien, die verfolgt werden.
Die ersten Krebstherapien, die zur Verfügung standen, waren die sogenannten Chemotherapeutika, die breit wirken und neben den Tumorzellen auch gesunde Zellen angreifen. Im Laufe der Zeit nahm zusätzlich die Entwicklung zielgerichteter Therapien stark zu. Diese erkennen bestimmte, für den Tumor typische Strukturen, wie zum Beispiel den HER2-Rezeptor, und wirken speziell auf diese Struktur.
Im Allgemeinen wirkt eine Chemotherapie gegen Zellen, die sich teilen. Dadurch, dass Krebszellen sich mehr und/oder schneller als andere Körperzellen teilen, wirkt die Chemotherapie auf die Krebszelle stärker als auf andere Körperzellen. Dennoch werden auch gesunde, sich teilende Körperzellen angegriffen, was zu bekannten Nebenwirkungen wie z.B. Haarausfall führen kann.
Wenn nun eine zielgerichtete Therapie eingesetzt wird, so werden im Idealfall nur noch die Tumorzellen angegriffen, die den spezifischen Angriffspunkt – die tumortypische Struktur – aufweisen. Bei der Entwicklung solcher zielgerichteten Therapien versucht man auf oder in Krebszellen eine Eigenschaft auszumachen, die nur bzw. überwiegend diese Krebszelle aufweist. Das kann zum Beispiel eine bestimmte Strukturveränderung (eine „Mutation“) sein, oder ein Protein, das diese Krebszelle außergewöhnlich stark produziert. Ein Wirkstoff, der spezifisch gegen diese Eigenschaft wirkt, wird als zielgerichtete Therapie bezeichnet. Auch diese Wirkstoffe haben zum Ziel, das Tumorwachstum zu hemmen und idealerweise den Zelltod herbeizuführen. Solche Angriffspunkte für zielgerichtete Therapien sind allerdings nicht ausschließlich typisch für den Tumor. Zum Beispiel kommt der HER2-Rezeptor (in sehr viel geringeren Mengen) auch in gesunden Zellen vor, was für unseren Körper auch wichtig ist. Zielgerichtete Therapien wirken daher in einem deutlich geringeren Maße auch auf gesunde Zellen, die denselben Angriffspunkt aufweisen. Dies kann ebenfalls zu Nebenwirkungen führen, die im Vergleich zu einer Chemotherapie jedoch meist milder ausfallen.
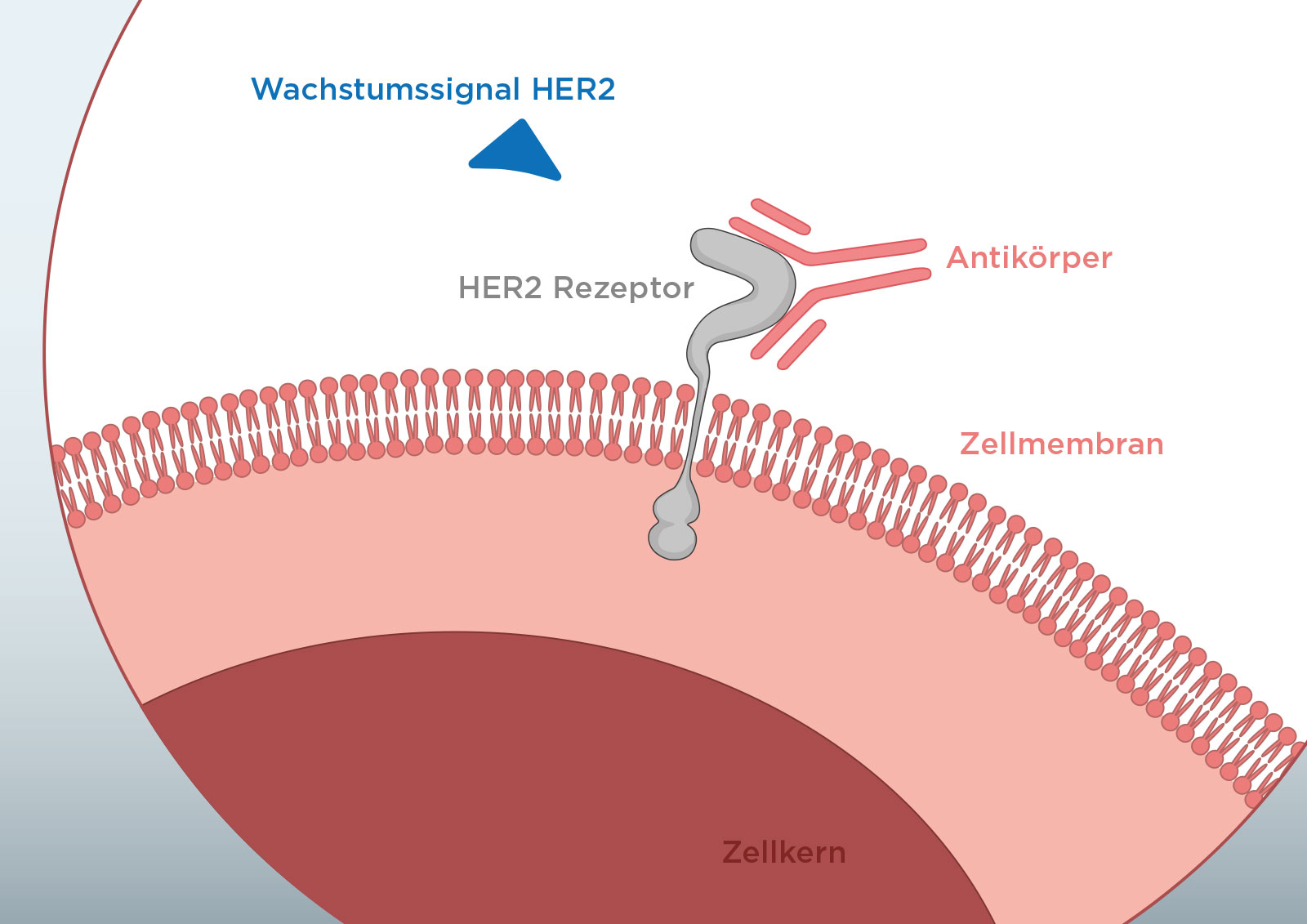
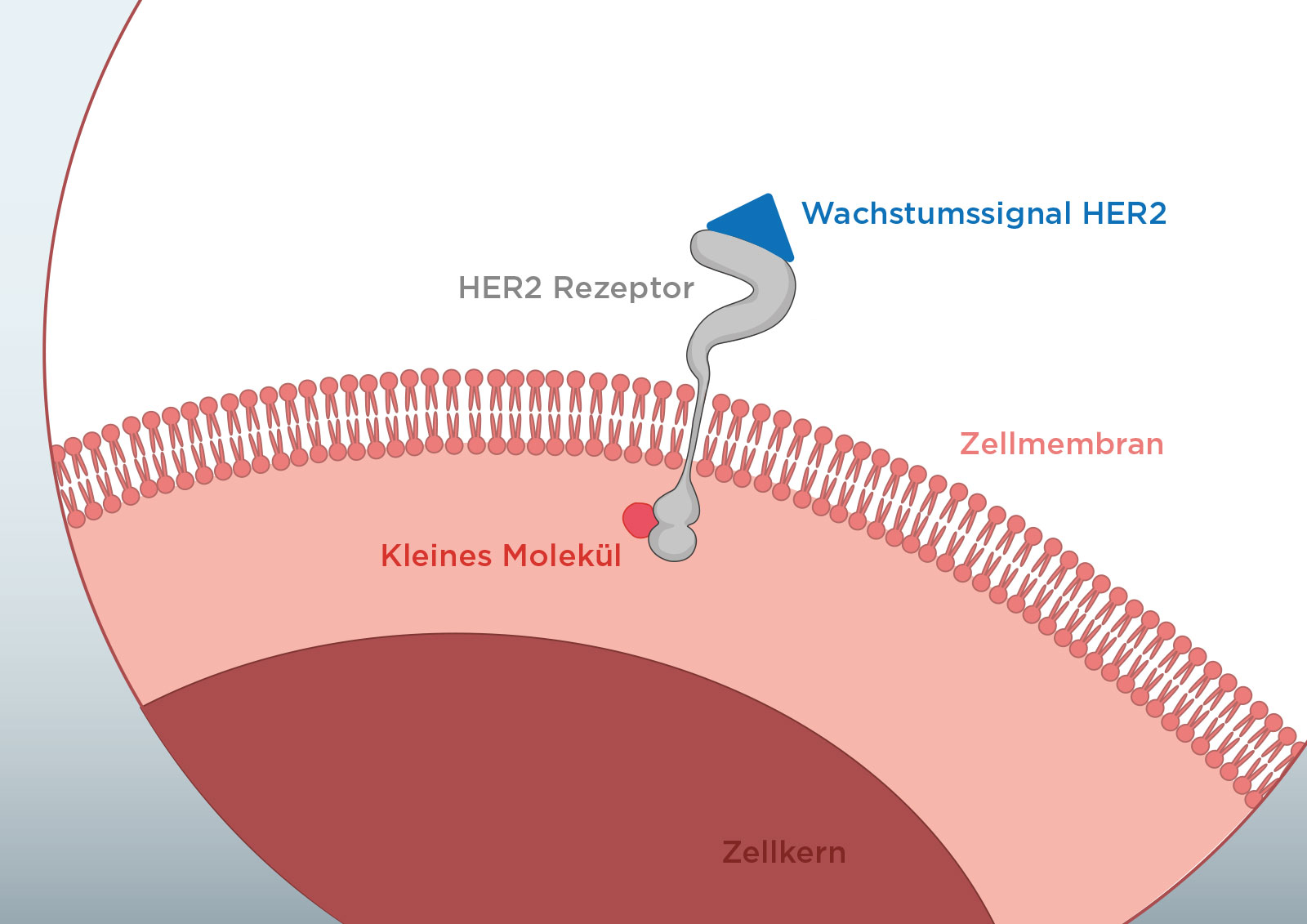
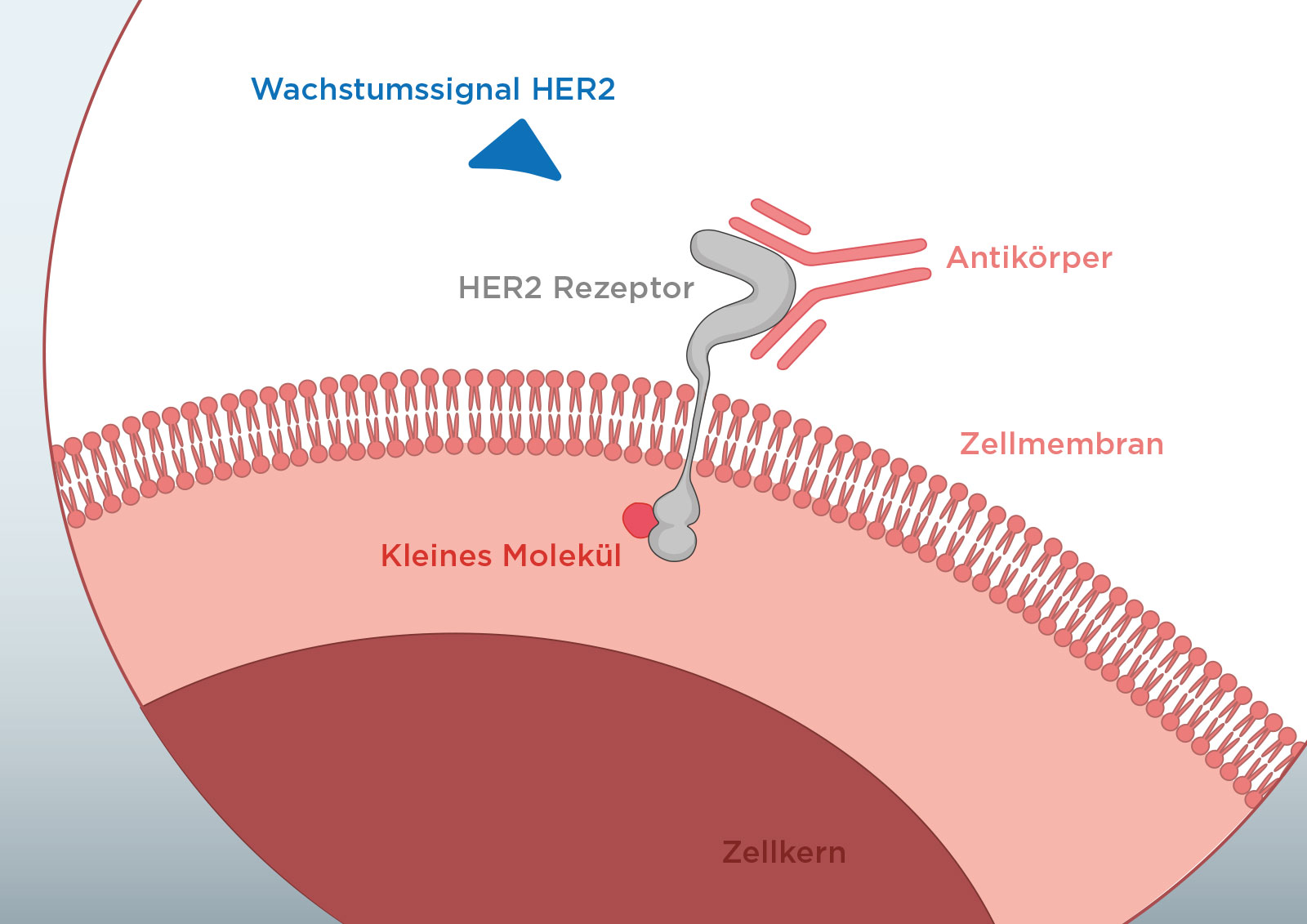
Zielgerichtete Therapien stehen in verschiedenen Formen zu Verfügung, z.B. als monoklonale Antikörper, die meist intravenös oder subkutan verabreicht werden, oder als kleine Moleküle, die zum Teil auch oral eingenommen werden können.
Nicht gegen jede Krebsart können zielgerichtete Therapien eingesetzt werden. Die Entscheidung, ob eine Therapie verfügbar ist und welche Therapie sinnvoll ist, hängt von vielen Faktoren ab. Ihr Arzt wird mit Ihnen zusammen die für Sie individuell bestmögliche Therapie auswählen.
Wirkstoffgruppen
Antikörper sind Proteine (Eiweiße), die an bestimmte Stellen anderer Proteine binden können. Dadurch sind sie in der Lage, die Funktion dieser Proteine - oftmals Enzyme oder sogenannte „Rezeptoren“ - zu hemmen. Beispielsweise kann die Bindung eines Antikörpers an ein Rezeptor-Protein, dessen Zweck das Auslösen eines Signals in der Zelle ist, diesen Signalfluss blockieren. Durch ihre Größe können Antikörper nicht in das Zellinnere eindringen.
Diese ähneln in ihrer Funktion Antikörpern, sind aber keine Proteine, sondern kleine chemische Moleküle. Dadurch können sie in das Innere einer Zelle gelangen, dort an bestimmte Proteine binden und deren Signalweiterleitung hemmen. Diese Proteine im Zellinneren, die Signale vermitteln und ein häufiges Ziel für diese Art von Medikamenten darstellen, heißen Kinasen (Eiweiße mit bestimmten Funktionen). Bei kleinen Molekülen mit dieser Wirkungsweise spricht man daher auch von „Kinasehemmern“.

Brustkrebs im Frühstadium - und jetzt?
In Deutschland erhalten über 70.000 Frauen pro Jahr die Diagnose Brustkrebs
Während jüngere Frauen nur selten betroffen sind, steigt das Risiko ab dem 40. und besonders ab dem 50. Lebensjahr an. Im Durchschnitt erkranken Frauen mit etwa 64 Jahren an Brustkrebs. Jede vierte Betroffene ist bei der Diagnose jünger als 55 Jahre und jede Zehnte jünger als 45 Jahre.
Die Diagnose Brustkrebs löst zunächst Ängste und Sorgen aus – verständlich, denn von einem auf den anderen Tag wird alles auf den Kopf gestellt. Wie geht es jetzt weiter? Die gute Nachricht ist: Brustkrebs ist heutzutage aufgrund der Früherkennung in vielen Fällen heilbar. Mediziner verstehen die Mechanismen der Krebsentstehung immer besser und können betroffene Frauen zunehmend effektiver behandeln. Vor allem bei erstmals aufgetretenem, lokal begrenztem Brustkrebs im Frühstadium ist die Erkrankung in vielen Fällen erfolgreich zu behandeln und die Chance, ein Wiederauftreten des Tumors zu vermeiden, groß.
Welche Therapie genau zum Einsatz kommt, entscheidet der behandelnde Arzt basierend auf verschiedenen Faktoren, wie z. B. der Größe des Tumors und der Ausbreitung der Krebserkrankung oder den Besonderheiten der Tumorzellen. Brustkrebs ist so individuell wie die Frau, die ihn hat. Mithilfe biologischer Tumormarker („Biomarker“) lässt sich zum einen erkennen, wie aggressiv ein Tumor ist und wie die Prognose aus sieht („prognostische Marker“). Zum anderen können Mediziner daraus ableiten, mit welcher Therapie sie den Tumor am besten bekämpfen können („prädiktive Marker“). Viele dieser Marker konnten Wissenschaftler schon entschlüsseln und es kommen immer weitere hinzu. Mediziner unterteilen Brustkrebs je nach Art des Entstehungsmechanismus in eine ganze Reihe von Subtypen – man spricht hierbei auch von der Tumorbiologie. Relevante Tumormarker sind beispielsweise der Hormonrezeptor (HR), der HER2-Rezeptor, oder auch Ki-67.
Ein weiterer wichtiger Marker ist der „HER2-Rezeptorstatus“, also das vermehrte Vorhandensein sogenannter HER2-Rezeptoren auf den Tumorzellen (HER2 aus dem Englischen: Humaner Epidermaler Wachstumsfaktor-Rezeptor 2). HER2-Rezeptoren können die Zelle zur Teilung anregen und vermitteln Signale, die das Überleben der (Tumor-)Zellen begünstigen können. Eine normale Zelle besitzt nur eine relativ geringe Menge an HER2-Rezeptoren. Man spricht dann von HER2-„negativen“ Zellen. Bei ca. 15 bis 20 Prozent aller Brusttumore ist jedoch die Anzahl der HER2-Rezeptoren auf der Zelloberfläche stark erhöht, in diesem Fall spricht man von HER2-„positiven“ (kurz HER2+) Tumorzellen bzw. Tumoren. Durch die Vielzahl an HER2-Rezeptoren wird die Teilungsrate der Zellen überdurchschnittlich aktiviert, was wiederum zu vermehrtem Tumorwachstum führt. Daher wird bei HER2-positiven Tumoren in den meisten Fällen eine zielgerichtete Therapie eingesetzt, die die Aktivität des HER2-Rezeptors blockiert.
Ein wichtiger Parameter für die Einteilung in verschiedene Subtypen ist der sogenannte Hormonrezeptorstatus. Dieser gibt Auskunft darüber, ob der Tumor auf Hormone wie Östrogen und Progesteron anspricht, sein Wachstum also durch die Hormone gefördert wird. Verfügen Krebszellen über eine hohe Anzahl von Bindungsstellen für Hormone, sogenannte Hormonrezeptoren (kurz: HR), so docken die Hormone an diese Rezeptoren an und lösen damit die Weiterleitung von Wachstumssignalen aus. In diesem Fall wächst der Tumor hormonabhängig, der Hormonrezeptor-„Status“ ist „positiv“ (HR+). Dies ist bei etwa zwei Drittel aller Brustkrebsarten der Fall. Des Weiteren lässt sich ermitteln, auf welche Hormone der Tumor reagiert, auf Östrogen (Östrogenrezeptor-positiv = ER+) und/oder auf Progesteron (Progesteronrezeptor-positiv = PgR+). Wenn ein Tumor hormonabhängig wächst, bedeutet dies im Umkehrschluss, dass sich sein Wachstum durch eine antihormonelle Therapie verlangsamen oder stoppen lässt.
Ist die Anzahl der Hormonrezeptoren im Tumor hingegen gering, so spricht man von einem „negativen“ Hormonrezeptorstatus (HR-).
Mit weiteren molekularbiologischen Tests lassen sich zusätzliche Informationen erhalten. Der Proliferationsmarker Ki-67 zum Beispiel gibt einen Hinweis auf die Wachstumsgeschwindigkeit von Tumorzellen.